时间总是匆匆易逝,转眼间10月份即将结束了,在即将过去的10月里,Nature杂志又有哪些亮点研究值得学习呢?小编对相关文章进行了整理,与大家一起学习
Nature:揭示蛋白BORIS是耐药性癌症产生的罪魁祸首
doi:10.1038/s41586-019-1472-0
在一项新的研究中,美国研究人员发现一种称为BORIS的蛋白是某些儿童癌症的罪魁祸首。这种蛋白能够破解神经母细胞瘤基因组,导致在某些类型的治疗后处于休眠状态的癌细胞苏醒过来,从而引起癌症复发。他们还发现这种蛋白与其他几种癌症中的耐药性相关,相关研究结果发表在Nature期刊上。

当细胞需要开启特定基因时,包裹我们DNA的长长的染色质纤维会形成环状结构。这些染色质环状结构让基因启动子和基因增强子靠得很近,从而使得一个基因或一组基因得以开启和表达。这项研究发现,在神经母细胞瘤中,BORIS形成并锚定了新的环状结构,同时开启了许多基因,但不是以一种好的方式。
Nature:重磅!科学家在人类癌症基因组非编码区域中鉴别出关键的致癌突变
doi:10.1038/s41586-019-1651-z
近日,一项刊登在国际杂志Nature上的研究报告中,来自加拿大安大略省癌症研究所的科学家们通过研究在人类癌症基因组中的大量非编码区域(也被称之为人类癌症DNA的“暗物质”)中发现了一种新型的致癌突变;这种突变或能作为一种新型潜在的治疗靶点,帮助科学家们开发治疗多种类型癌症的新型疗法,包括脑癌、肝癌和血液癌症等。
研究者Lincoln Stein表示,非编码DNA在基因组中占到了98%的比例,其对于科学家们而言非常难以研究,而且其因为不编码蛋白质经常会被忽略。通过仔细分析这些区域,研究人员在DNA代码的一个碱基中发现了改变,其或能驱动多种类型癌症的发生,研究人员或能利用这种新型癌症机制来开发治疗包括癌症在内多种疾病的新型疗法。

Nature:揭示α-酮戊二酸是p53介导的肿瘤抑制的效应因子
doi:10.1038/s41586-019-1577-5
肿瘤抑制基因TP53(编码蛋白p53)在大多数人类癌症中以及在70%以上的胰腺导管腺癌(PDAC)中发生突变。野生型p53在细胞应激反应中积累,并调节基因表达以改变细胞命运和阻止肿瘤产生。众所周知,野生型p53也可以调节细胞代谢途径,不过人们对p53依赖性的抑制癌症进展的代谢变化仍然知之甚少。
在一项新的研究中,来自美国纪念斯隆凯特琳癌症中心等研究机构的研究人员发现p53重塑癌细胞代谢,从而促进染色质和基因表达发生有利于维持癌变前细胞命运(premalignant cell fate)的变化。在源自发生KRAS突变的PDAC小鼠模型的癌细胞中恢复p53功能导致α-酮戊二酸(αKG)积累,其中αKG也可作为一部分染色质修饰酶的专一性底物,相关研究结果发表在Nature期刊上。
Nature封面文章:尼古丁成瘾性或与2型糖尿病风险增加密切相关!
doi:10.1038/s41586-019-1653-x
近日,一项刊登在国际杂志Nature上的研究报告中,来自西奈山医学院的研究人员通过研究在大鼠机体中发现了一种特殊回路,或能将吸烟和2型糖尿病患病风险相联系起来。相比非吸烟者而言,糖尿病在吸烟人群中往往更加流行,但其背后的原因研究者尚不清楚。文章中,研究者发现,尼古丁的摄入或能通过一种大脑回路与胰腺的活性相关,摄入尼古丁会引发胰腺释放较少量的胰岛素,从而增加机体血糖水平,较高的血糖水平与糖尿病风险增加直接相关。
研究者发现,糖尿病相关基因Tcf7l2(转录因子7类似物2)所编码的特殊蛋白能介导一种信号回路,从而将尼古丁激活的神经元与胰腺血糖调节相联系起来;尼古丁能够激活大脑内侧缰核区域中神经元所表达的尼古丁乙酰胆碱受体(nAChR),从而引发尼古丁的不良反应,限制胰腺对胰高血糖素和胰岛素的吸收和释放,从而提高血糖水平;较高的血糖水平能通过抑制表达nAChR的神经元来产生一种反馈回路,阻断吸烟的负面效应,并帮助建立尼古丁依赖性;Tcf7l2能调节整个信号回路,并将尼古丁成瘾性与糖尿病高风险相关联。
Nature:新研究首次揭示抑制年龄相关的神经活动增加竟可延长寿命
doi:10.1038/s41586-019-1647-8
在一项针对线虫、小鼠和人类的研究中,来自美国哈佛医学院的研究人员发现在整个动物界中,衰老会带来更多的神经活动,而当这种自然增加受到限制时,个体的寿命可能就会变得更长。他们着重介绍了一种保守性的称为REST的转录因子,它可能是调节这种年龄相关的神经活动的关键,相关研究结果发表在Nature期刊上。
在美国韦恩州立大学研究线虫和果蝇衰老的Joy Alcedo(也未参与这项研究)补充说,“这是一个令人着迷的观点:随着人们年龄的增加,我们的神经元可能实际上变得更加活跃,而且简单地抑制这种神经活动可能就足以延长寿命。”研究者Bruce Yankner说,随着人们的年龄增长,大脑中的基因表达方式会以非随机的方式发生变化,从而使得年轻人和老年人可通过其转录特征来加以区分。当然,所有老年人都不一样,有些人健康,有些则不那么健康。Yankner及其同事们对某些表达特征是否与这种差异相关感兴趣。
图片来源:Nature, 2019, doi:10.1038/s41586-019-1646-9
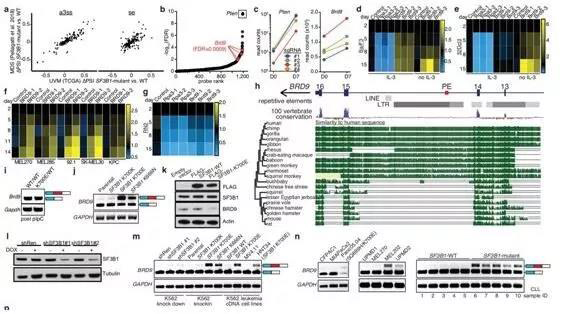
Nature:重大进展!新研究揭示最常见的SF3B1基因突变如何导致癌症
doi:10.1038/s41586-019-1646-9
在一项新的研究中,来自美国弗雷德哈金森癌症研究中心和纪念斯隆凯特琳癌症中心等研究机构的研究人员确定了SF3B1(splicing factor 3b subunit 1, 剪接因子3b亚基1)基因突变如何促进很多癌症形成,其中SF3B1是最为频繁发生突变的剪接因子编码基因,相关研究结果近期发表在Nature期刊上。
这些研究人员发现了SF3B1基因突变如何导致癌症,这些突变发生在许多癌症类型中,包括各种白血病、骨髓增生异常综合征、黑色素瘤、乳腺癌、胰腺癌、肝癌和膀胱癌。鉴于SF3B1编码的蛋白对于产生RNA分子至关重要,因此Bradley和Abdel-Wahab研究了来自数百名患有几种不同癌症类型的患者的RNA测序数据,以寻找异常的RNA分子。他们发现SF3B1突变导致癌细胞产生异常形式的BRD9 RNA分子,它包括非编码DNA序列或者说“垃圾DNA”。
这种“垃圾DNA”源自近期将自身插入人类基因组的病毒序列元件。 Bradley和Abdel-Wahab发现BRD9在许多类型的癌症中都是重要的肿瘤抑制因子,这些癌症包括葡萄膜黑色素瘤(一种影响眼睛的黑色素瘤类型)、慢性淋巴细胞性白血病和胰腺癌。他们随后利用CRISPR技术和反义寡核苷酸设计了可逆转这种疾病过程的疗法。
Nature:世界上首个三类器官系统为医学研究和诊断打开了大门
doi:10.1038/s41586-019-1598-0
器官发生是一个复杂的、相互联系的过程,是由多种边界组织相互作用所协调的。但是,人们尚不清楚各个相邻的组成部分如何协调以建立一个完整的多器官结构。
在一项新的研究中,来自美国辛辛那提儿童医学中心和日本东京医科牙科大学的研究人员报道肝脏、胆管和胰腺结构的连续模式和动态形态发生,这些结构是由人多能性干细胞的三维培养物内陷形成的。由人多能性干细胞分化而来的前肠球状体和后肠球状体之间的边界相互作用使得肝脏-胆管-胰腺结构在没有外来因素的情形下在前肠-中肠边界的类器官上发生特化而形成,这种形成依赖于视黄酸,相关研究结果发表在Nature期刊上。
Nature:中荷科学家联手揭示“连续左右拳击”可杀死癌细胞
doi:10.1038/s41586-019-1607-3
作为一个经典的拳击动作,“连续左右拳击(one-two punch)”也可能对癌症有效:左拳将癌细胞击昏,紧接着是右拳将癌细胞击倒。在一项新的研究中,来自中国上海交通大学和荷兰癌症研究所的研究人员发现癌细胞很容易受到这种方法的攻击。“这是一条美妙的通用原则,可以用于所有形式的癌症,相关研究结果发表在Nature期刊上。
从理论上讲,许多抗癌药物组合使用可以很好地协同发挥作用,但实际上,这些组合使用的毒性太大,人体无法承受。这些研究人员设计出一种可能的替代方法:“连续左右猛击”,以拳击中两次快速连续拳击的有效结合而得名。“第一种药物在癌细胞中产生弱点,第二种药物对暴露弱点的癌细胞进行无情打击。因此,尽管这两种药物不是同时使用,但是仍然能够从它们的协同作用中受益。
Nature:新一代CRISPR基因编辑技术诞生,或为人体细胞提供多种功能
doi:10.1038/s41586-019-1711-4
近日,来自美国布罗德研究所的科学家们通开发了一种新的CRISPR基因组编辑方法,能够进一步提高基因编辑的效率与准确性。该系统称为“prime editing”,能够以精确,高效和高度通用的方式直接编辑人体细胞。该方法扩大了生物学和治疗学研究的基因编辑范围,并有可能校正多达89%的已知致病基因变异。
“分子生命科学的主要宗旨是能够达到在任何位置精确地改变基因组的能力。我们认为这一新开发的基因编辑技术使我们离这一目标更近”,该研究的作者之一David Liu说到。prime editing”不同于以前的基因组编辑系统。
Cas9蛋白是最早在人类细胞中进行基因组编辑的CRISPR工具,它是由布罗德研究所,麻省理工学院和哈佛大学率先开发。Cas9能够切割DNA链,从而可以在特定位置破坏靶基因,然后通过将新的DNA重组到靶位点而添加新的序列。
Nature:首次绘制人类发育中肝脏的细胞图谱,破解人类胎儿肝脏造血秘密
doi:10.1038/s41586-019-1652-y
在一项新的研究中,英国研究人员在世界上首次构建出人类发育中肝脏的细胞图谱,它提供了关于胎儿中血液和免疫系统如何产生的重要见解。这种图谱描绘了在妊娠的头三个月和第二个三个月之间的发育中肝脏的细胞景观变化,包括来自肝脏的干细胞如何播种到其他组织,以支持生长所需的高氧气需求,相关研究结果发表在Nature期刊上。
这种图谱是一种综合的高分辨率资源,可改进我们对正常发育的理解,并且有助于医疗机构治疗可能在发育过程中形成的疾病,比如白血病和免疫疾病。在此之前,人们还不清楚人类血液和免疫系统如何产生,这一过程被称为造血作用。成年后,正是骨髓产生我们的血液和免疫细胞。但是在早期胚胎生活中,卵黄囊和肝脏在制造血液和免疫细胞中起着重要作用。这些细胞随后播种到外周组织,比如皮肤、肾脏,最终播种到骨髓。
转载于生物谷





 浙公网安备33010802007965号
浙公网安备33010802007965号